Zęby martwe
Zdrowy ząb to żywy organ
Zdrowy ząb to żywy organ. Tworzą go trzy tkanki: szkliwo, zębina i miazga. Szkliwo jest twardą tkanką ochronną, składającą się w 96% z materii nieorganicznej. Nie jest ono ukrwione ani unerwione.
Zębina to tkanka miękksza niż szkliwo, wrażliwa na ból i stanowiąca główny budulec zęba. Składa się w 70% z materii nieorganicznej. Resztę stanowią białka, tłuszcze i komórki zwane odontoblastami. Ma strukturą przypominającą gąbkę – przenika ją bardzo gęsta (20 000 – 50 000 / cm2) sieć kanalików o średnicy 1 do 2.5 mikronów. W zdrowym zębie zachodzi w niej wiele procesów obronnych i regeneracyjnych.
Miazga to tkanka miękka wypełniająca komorę zębową. Znajduje się w niej wiele różnych komórek i białek a także naczyń krwionośnych, limfatycznych i nerwów (zarówno z układu czuciowego jak i autonomicznego). Główną rolą miazgi jest odżywianie i modulowanie reakcji obronnych zęba a tym samym utrzymanie go przy zdrowiu i “życiu”. To od stanu miazgi zależy żywotność zęba.
Ząb otoczony jest tkankami przyzębia, będącymi z nim w ścisłym związku strukturalnym i funkcjonalnym.
Leczenie kanałowe – na czym polega?
Kiedy równowaga procesów zachodzących w szkliwie i zębinie zostanie zachwiana, a ząb ulegnie zniszczeniu przez próchnicę lub mechanicznemu uszkodzeniu dochodzi do zapalenia miazgi a z czasem do obumarcia zęba. W takim wypadku najczęściej proponowane jest leczenie kanałowe. Polega ono na mechanicznym usunięciu miazgi z komory i kanałów zęba, następnie oczyszczeniu ich, zdezynfekowaniu i wypełnieniu. W ten sposób usuwa się źródło infekcji z miazgi i częściowo z otaczającej jej zębiny. Lecz mimo, że leczenie wykonywane jest bardzo precyzyjnie, nie sposób jest dotrzeć do każdego kanalika zębinowego. Poprawnie wykonane leczenie kanałowe pozwala na wyeliminowanie bólu spowodowanego zapaleniem miazgi i zachowanie twardych tkanek zęba, ale nie zawsze eliminuje źródło infekcji.
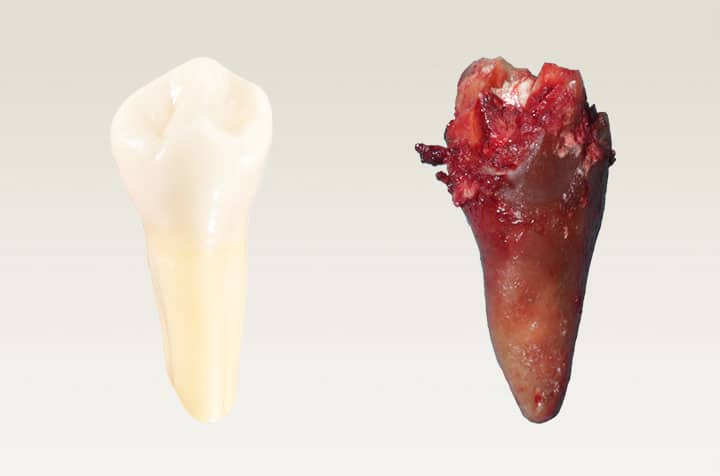
Zęby martwe a zdrowie ogólne
Ząb martwy nie ma już możliwości własnej obrony a reakcja układu immunologicznego jest dodatkowo utrudniona trudnym dostępem do źródła infekcji, wynikającej z anatomii zęba. Ząb staje się miejscem zasiedlenia beztlenowych, patogennych bakterii.
Produkują one różne toksyczne produkty metaboliczne. Przykładem takich toksyn są potencjalnie rakotwórcze siarkowodory tioeter i merkaptan z aminokwasów cysteiny i metioniny. Przy każdym nacisku na ząb toksyny są przemieszczane do otaczających tkanek i dalej do krwi. Wpływ tych związków na zdrowie człowieka może być różny, lecz na pewno nie pozytywny. Wiadomo jednak, że nawet w minimalnych stężeniach, związki te mogą niszczyć enzymy. Dezaktywacja tych niezbędnych enzymów może prowadzić do wielu hormonalnych, neurologicznych czy autoimmunologicznych chorób. Toksyny uwalniające się z zęba stanowią też stałe obciążenie dla układu odpornościowego.
Poza tym często dochodzi do często asymptomatycznego, ostrego miejscowego zapalenia kości i innych tkanek przyzębia otaczających wierzchołek korzeń zęba martwego (okołowierzchołkowe zapalenie kości), w wyniku którego dochodzi do zaniku kości i co również grozi rozprzestrzenieniem się infekcji.

Leczenie
Skutecznym sposobem na kompletne wyeliminowanie bakterii znajdujących się w zębie martwym i uniemożliwienie im ponownego zasiedlenia tego zęba jest usunięcie go i oczyszczenie otaczających go tkanek przyzębia. Oczywiście pozostaje też opcja leczenia kanałowego, która najczęściej usunie ostry stan zapalny i dolegliwości bólowe związane z tym stanem zapalnym, lecz nie gwarantuje całkowitego wyeliminowania infekcji.
Badania i źródła do powyższego tekstu
- Jacobi-Gresser E, Schütt S, Huesker K, Baehr V v. Methyl mercaptan and hydrogen sulfide products stimulate proinflammatory cytokines in patients with necrotic pulp tissue and endodontically treated teeth. J Biol Regul Homeost Agents. 2015;29(1):73–84.
- Kwang S, Abbott P. The presence and distribution of bacteria in dentinal tubules of root filled teeth. Int Endod J. 2014;47(6):600–10. doi:10.1111/iej.12195
- Lechner J, Baehr V v. Impact of Endodontically Treated Teeth on Systemic Diseases. Dentistry. 2018;08(03). doi:10.4172/2161-1122.1000476
- Gomes C, Martinho FC, Barbosa DS, Antunes LS, Póvoa HCC, Baltus THL, Morelli NR, Vargas HO, Nunes SOV, Anderson G, Maes M. Increased Root Canal Endotoxin Levels are Associated with Chronic Apical Periodontitis, Increased Oxidative and Nitrosative Stress, Major Depression, Severity of Depression, and a Lowered Quality of Life. Molecular Neurobiology. 2018;55(4):2814–27. doi:10.1007/ s12035-017-0545-z
- Lechner J, Baehr V v. Stimulation of proinflammatory cytokines by volatile sulfur compounds in endodontically treated teeth. Int J Gen Med. 2015;8109–18. doi:10.2147/ IJGM.S77693
- Siqueira JF, Rôças IN, Alves FRF, Silva MG. Bacteria in the apical root canal of teeth with primary apical periodontitis. Oral Surg Oral Med Oral Pathol Oral Radiol Endod. 2009;107(5):721–6. doi:10.1016/j.tripleo.2009.01.042
- Vahlkamp T, Meijer AJ, Wilms J, Chamuleau RA. Inhibition of mitochondrial electron transfer in rats by ethanethiol and methanethiol. Clin Sci. 1979;56(2):147–56. doi:10.1042/ cs0560147
- IMD Berlin. Labordiagnostik bei chronisch entzündlichen Multisystemerkrankungen [Internet] . Available from: https://www.imd-berlin.de/fachinformationen/diagnostikinformationen/entzuendungsdiagnostik-bei-multisystemerkrankungen.html
- Richardson N, Mordan NJ, Figueiredo JAP, Ng Y-L, Gulabivala K. Microflora in teeth associated with apical periodontitis: a methodological observational study comparing two protocols and three microscopy techniques. Int Endod J. 2009;42(10):908–21. doi:10.1111/j.1365-2591.2009.01594.x
- Cotti E, Dessì C, Piras A, Flore G, Deidda M, Madeddu C, Zedda A, Longu G, Mercuro G. Association of endodontic infection with detection of an initial lesion to the cardiovascular system. Journal of Endodontics. 2011;37(12):1624–9. doi:10.1016/j.joen.2011.09.006
- Cotti E, Dessì C, Piras A, Mercuro G. Can a chronic dental infection be considered a cause of cardiovascular disease? A review of the literature. Int J Cardiol. 2011;148(1):4–10. doi:10.1016/j.ijcard.2010.08.011
- Bains R, Bains VK. Lesions of endodontic origin: An emerging risk factor for coronary heart diseases. Indian Heart J. 2018;70 Suppl 3S431-S434. doi:10.1016/j. ihj.2018.07.004
- Ganzimmun Diagnostics AG. Endotoxinämie: LPS im Serum als Marker für Silent Inflammation. 2015;(Fachinformation 0086):1-11.
- Dr. Elisabeth Jacobi-Gresser. Risiken für chronische Entzündungen durch orale Reizfaktoren: Immunlabordiagnostik in der Zahnheilkunde. ZMK Allgemeine Zahnheilkunde. 2012.
- Aminoshariae A, Kulild JC, Mickel A, Fouad AF. Association between Systemic Diseases and Endodontic Outcome: A Systematic Review. Journal of Endodontics. 2017;43(4):514–9. doi:10.1016/j.joen.2016.11.008
- Murray CA, Saunders WP. Root canal treatment and general health: a review of the literature. Int Endod J. 2000;33(1):1–18. doi:10.1046/j.1365-2591.2000.00293.x
- Liljestrand JM, Mäntylä P, Paju S, Buhlin K, Kopra KAE, Persson GR, Hernandez M, Nieminen MS, Sinisalo J, Tjäderhane L, Pussinen PJ. Association of Endodontic Lesions with Coronary Artery Disease. J Dent Res. 2016;95(12):1358– 65. doi:10.1177/0022034516660509
- Segura-Egea JJ, Martín-González J, Castellanos-Cosano L. Endodontic medicine: connections between apical periodontitis and systemic diseases. Int Endod J. 2015;48(10):933–51. doi:10.1111/iej.12507
- Goon ATJ, Isaksson MAI. Hand Eczema from Acrylate Compounds in Dentistry. In: Alikhan A, Lachapelle J-M, Maibach HI, editors. Textbook of Hand Eczema. Berlin, Heidelberg: Springer Berlin Heidelberg; 2014. p. 169–83. (vol. 34).
- Mjör IA, Nordahl I. The density and branching of dentinal tubules in human teeth. Archives of Oral Biology. 1996;41(5):401–12. doi:10.1016/0003-9969(96)00008-8
- Merkur.de. Diese Viren und Bakterien machen uns krank: Sie sind unsichtbar, aber überall: Viren und Bakterien machen uns krank. Doch die beiden Erreger haben sonst wenig gemeinsam. Warum sie sich unterscheiden. [Internet]. 2017. Available from: https://www.merkur.de/leben/ gesundheit/viren-bakterien-sind-menschen-gefaeh-
- rlich-virusinfektion-zr-4417390.html
- Dr. Elisabeth Jacobi-Gresser. Risiken für chronische Entzündungen durch orale Reizfaktoren: Immunlabordiagnostik in der Zahnheilkunde. ZMK Allgemeine Zahn- heilkunde. 2012.
- CaiX,CaoC,LiJ,ChenF,ZhangS,LiuB,ZhangW, Zhang X, Ye L. Inflammatory factor TNF-α promotes the growth of breast cancer via the positive feedback loop of TNFR1/NF-κB (and/or p38)/p-STAT3/HBXIP/TNFR1. Oncotarget. 2017;8(35):58338–52. doi:10.18632/oncotarget.16873
- Wolczyk D, Zaremba-Czogalla M, Hryniewicz-Jankowska A, Tabola R, Grabowski K, Sikorski AF, Augoff K. TNF-α promotes breast cancer cell migration and enhances the concentration of membrane-associated proteases in lipid rafts. Cell Oncol (Dordr). 2016;39(4):353–63. doi:10.1007/ s13402-016-0280-x
